La inmunoterapia después de quimioterapia de alta dosis ofrece resultados favorables en la leucemia mieloide aguda
Un ensayo clínico ha descubierto que la quimioterapia en dosis altas seguida de un tratamiento posterior de inmunoterapia benefició a los pacientes con leucemia mieloide aguda (LMA) resistente o en recaída, un cáncer muy agresivo, según publican sus autores en la revista `Blood Cancer Discovery`, de la Asociación Americana de Investigación del Cáncer.
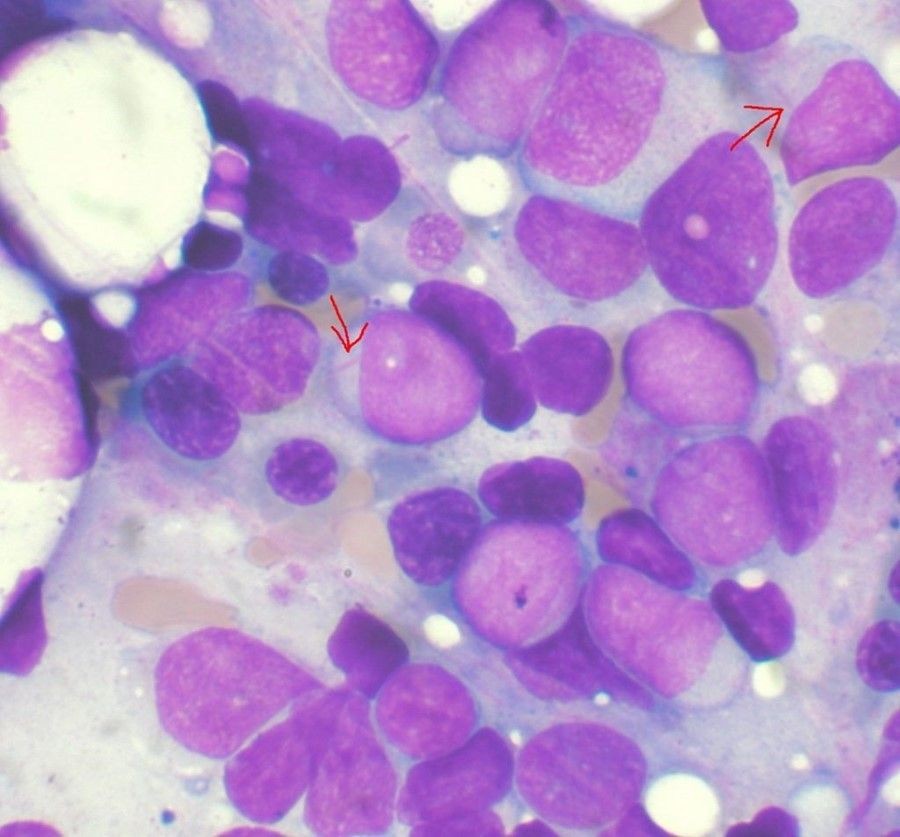
En el ensayo de fase II, realizado en el Centro Oncológico Integral Lineberger de la Universidad de Carolina del Norte (UNC) y en el Centro Oncológico Integral Sidney Kimmel de la Johns Hopkins, en Estados Unidos, participaron 37 pacientes menores de 70 años.
Recibieron inyecciones de alta dosis de quimioterapia con citarabina seguidas de inmunoterapia con pembrolizumab intravenoso dos semanas después para examinar si las respuestas clínicas pueden mejorar con la adición de pembrolizumab. En el punto final primario del ensayo, 14 personas (el 38%) tuvieron una remisión completa de su cáncer.
Estos resultados se comparan favorablemente con las tasas de remisión observadas con altas dosis de citarabina y otros regímenes de quimioterapia en la LMA resistente o recidivante. Y lo que es mejor, en los pacientes que no se habían beneficiado del tratamiento estándar y que recibieron altas dosis de citarabina seguidas de pembrolizumab en su segunda fase de tratamiento general, el 46% de los participantes en el ensayo lograron una remisión completa con el doble golpe, lo que sugiere que este tratamiento podría ser mejor al principio de la enfermedad. Los efectos secundarios graves fueron escasos y limitados.
"La inmunoterapia ha supuesto un cambio de paradigma en el tratamiento del cáncer, pero la LMA ha quedado rezagada respecto a otros tipos de cáncer, a pesar de los numerosos datos que indican que puede ser eficaz --afirma el doctor Joshua Zeidner, profesor asociado de Medicina, jefe de Investigación sobre la Leucemia en el UNC Lineberger y autor correspondiente de este estudio--. Nuestro estudio es el primer ensayo clínico que investiga el papel de pembrolizumab en combinación con quimioterapia intensiva en pacientes con LMA que recae o es resistente a la terapia".
Si bien la supervivencia a cinco años de la LMA ha pasado de alrededor del seis por ciento en 1975 a casi el 30 por ciento en la actualidad, la supervivencia en los estadios avanzados de la enfermedad sigue siendo escasa.
Los pacientes cuyo cáncer no responde a un tratamiento agresivo o se vuelve resistente a la quimioterapia suelen tener una esperanza de vida que se mide en meses, lo que hace que la búsqueda de mejores terapias sea una necesidad acuciante.
"En general, los participantes en el ensayo vivieron una media de casi un año después de su terapia, lo que es significativo en comparación con los beneficios anteriores observados con la quimioterapia sola, que dio lugar a una supervivencia media de seis a siete meses", añade Zeidner.
Además de encontrar el beneficio de la quimioterapia seguida de la inmunoterapia, los médicos descubrieron que un tipo específico de célula del sistema inmunitario, conocida como célula T, prevalecía antes del tratamiento.
El beneficio del tratamiento se correlacionó con la función de estas células T, ya que posiblemente una determinada población de células T pudo ser revigorizada por el pembrolizumab.
La presencia de estas células T puede ser capaz de predecir qué pacientes se benefician de pembrolizumab en la LMA. Además, diferentes vías genéticas eran más prevalentes en las células leucémicas de quienes respondían a pembrolizumab, lo que sugiere que estos genes podrían servir como potenciales biomarcadores para predecir la respuesta.
"Esperamos que los resultados de este estudio conduzcan a un ensayo clínico de quimioterapia con o sin inmunoterapia. También esperamos identificar biomarcadores robustos de respuesta a la inmunoterapia que puedan incorporarse a los diseños de futuros estudios --afirma el doctor Jonathan S. Serody, catedrático de Medicina Elizabeth Thomas, director del Programa de Terapia Celular de la UNC Lineberger y uno de los autores principales del estudio--. Además, estamos planeando incorporar nuestros resultados en un análisis más amplio y multiinstitucional de biomarcadores predictivos y características de respuesta a la inmunoterapia en la LMA".
En un comentario adjunto, el doctor James Allison, galardonado con el Premio Nobel en 2018 por su investigación sobre el aprovechamiento del sistema inmunitario para atacar el cáncer, y tres colegas del Centro Oncológico MD Anderson de la Universidad de Texas, escriben que "los resultados de este ensayo demuestran el potencial de las combinaciones racionalmente diseñadas de quimioterapia citotóxica con bloqueo de puntos de control inmunitarios para tratar neoplasias malignas históricamente refractarias, incluida la LMA recidivante y refractaria".
"Si bien la combinación parece aportar beneficios (desplaza la curva de supervivencia hacia la derecha en comparación con el historial), aún necesitamos inducir respuestas duraderas a largo plazo similares a las observadas en otras indicaciones para que la terapia de puntos de control pase a primer plano en la LMA", concluye.
Este estudio es el resultado de una colaboración entre investigadores clínicos y traslacionales de la UNC Lineberger, Johns Hopkins y Merck & Co, que apoyó el ensayo clínico y las evaluaciones de las células tumorales e inmunitarias en los pacientes tratados con esta terapia.
"Este tipo de investigación en colaboración, en la que dos centros oncológicos excepcionales trabajan con una empresa farmacéutica líder para trasladar racionalmente las terapias a la clínica, es fundamental para mejorar el resultado de los pacientes con leucemia mieloide aguda", declara Serody, que dirigió la colaboración.
Se están realizando estudios para explorar el papel de las inmunoterapias con un agente quimioterapéutico diferente, la azacitidina. Los investigadores también podrían explorar el uso de agentes de inmunoterapia distintos del pembrolizumab en futuros estudios.



























Sé el primero en comentar