La biología sintética de alto rendimiento podría ayudar a acelerar las futuras terapias génicas
Los virus adenoasociados (VAA) se han convertido en el vehículo ideal para suministrar carga genética terapéutica a los tejidos objetivo para la reciente ola de terapias genéticas que se están desarrollando en laboratorios de biotecnología. Pero los VAA naturales no se dirigen específicamente a células y tejidos enfermos, y el sistema inmunitario puede reconocerlos, lo que limita el éxito terapéutico.
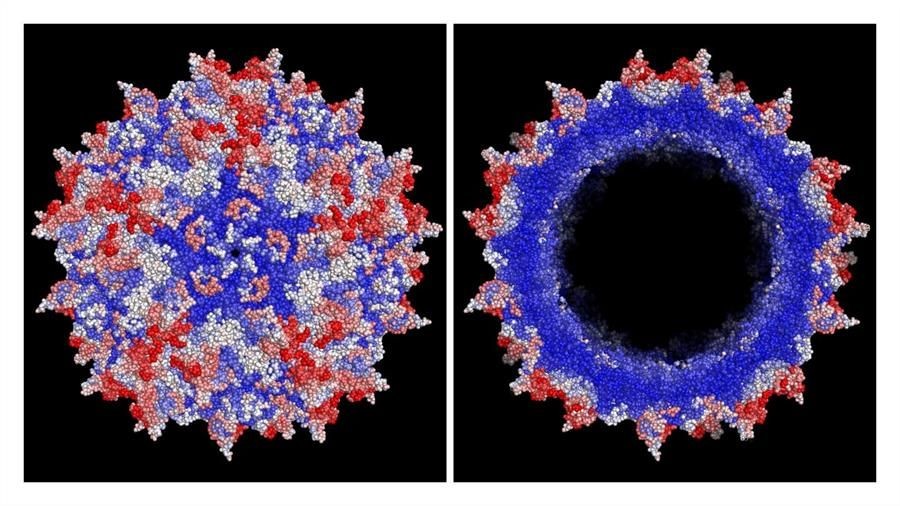
Ahora, los científicos del Instituto Wyss de Harvard para Ingeniería Biológicamente Inspirada y la Escuela de Medicina de Harvard (HMS) informan sobre un enfoque para acelerar el proceso de hacer tales cápsides de VAA mejoradas y desarrollar virus aún mejores, según publican en la revista Sus hallazgos se informan en \'Science\'.
Tomando un enfoque diferente y más sistemático para el problema de ingeniería de proteínas de la cápsida, el equipo muta uno por uno de cada uno de los 735 aminoácidos dentro de la cápsida de VAA2, el miembro más conocido de la familia de VAA, incluyendo todas las posibles sustituciones de codones, inserciones y deleciones en cada posición.
Generaron así una biblioteca de virus que contenía alrededor de 200.000 variantes e identificaron cambios en la cápside que mantuvieron la viabilidad de VAA2 y mejoraron su potencial de "retorno" (tropismo) a órganos específicos en ratones. Inesperadamente, el equipo también descubrió una nueva proteína accesoria oculta dentro de la secuencia de ADN que codifica la cápside que se une a la membrana de las células diana.
El equipo dirigido por el miembro de la Facultad Core de Wyss, George Church, y su ex becario postdoctoral Eric Kelsic, desplegaron un avanzado arsenal de biología sintética que incluye síntesis de ADN, código de barras y capacidades de secuenciación de ADN de próxima generación para construyendo una de las bibliotecas de cápsides VAA más completas hasta la fecha.
"Con la información generada por esta biblioteca, también pudimos diseñar cápsides con más mutaciones que las variantes naturales o sintéticas anteriores, y además con eficiencias de generar cápsidas viables que superan con creces las de AAV creadas por enfoques de mutagénesis aleatoria", señala Church, líder de la plataforma de biología sintética del Instituto Wyss.
"Estas tecnologías de alto rendimiento combinadas con un diseño guiado por máquina sientan las bases para diseñar variantes de VAA superiores y altamente personalizadas para futuras terapias génicas", señala el coautor Eric Kelsic, quien ahora es CEO de Dyno Therapeutics.
"Los enfoques anteriores, como el diseño racional o la mutagénesis aleatoria, tenían sus inconvenientes, ya sea limitado en el tamaño de la biblioteca o de baja calidad, respectivamente. El diseño guiado por máquina es un enfoque basado en datos para la ingeniería de proteínas --añade--. Aquí mostramos que incluso un el modelo matemático simple, impulsado por suficientes datos, puede generar con éxito cápsidas sintéticas viables. Este enfoque iterativo y empírico para la ingeniería de proteínas nos permite obtener lo mejor de ambos mundos y generar grandes cantidades de variantes de cápsidas de alta calidad".
"Inesperadamente, los datos de alta resolución que generamos nos permitieron detectar una nueva proteína codificada por un marco de lectura diferente dentro de la secuencia de ADN de la cápside, que había pasado desapercibida a pesar de décadas de intensa investigación sobre el virus", continúa el coautor Pierce Ogden, exestudiante de posgrado y ahora becario postdoctoral que trabaja con Church.
"La proteína accesoria asociada a la membrana (MAAP), como la llamamos, existe en todos los serotipos de AAV más populares y creemos que juega un papel en el ciclo de vida natural del virus --añade--. Estudiar cómo funciona MAAP será un área emocionante para investigación futura y podría conducir a una mejor comprensión de cómo producir y diseñar mejor las terapias genéticas AAV".
Según el coautor Sam Sinai, un exestudiante graduado de Church, ahora un científico de Machine Learning en Dyno Therapeutics, "esto revela la promesa de la ingeniería de proteínas basada en datos, en particular para proteínas como la cápside AAV que son difíciles de modelar con los enfoques computacionales actuales. Nuestros resultados son muy alentadores, pero también son solo un primer paso. Usando estos datos y los de futuros experimentos, construiremos modelos de aprendizaje automático para optimizar las cápsidas y abordar una amplia variedad de desafíos de terapia génica".
Kelsic, Sinai e Church son cofundadores de Dyno Therapeutics Inc. "Este estudio es un hito en el esfuerzo de la plataforma de Biología Sintética del Instituto Wyss para avanzar la tecnología AAV al siguiente nivel. Este trabajo también es un gran ejemplo de cómo estamos comenzando a integrar el aprendizaje automático y los enfoques de inteligencia artificial en nuestra línea terapéutica", señala.




























Sé el primero en comentar